Cancer du sein
Tout savoir sur le cancer du sein
L’Institut de Cancérologie de Lorraine prend en charge toute patiente atteinte d’un cancer du sein au sein de son parcours coordonné dédié.
Le parcours Sein permet de proposer aux personnes pour lesquelles une maladie du sein est suspectée d’avoir un diagnostic rapide. Les patients sont pris en charge par une équipe pluridisciplinaire spécialisée, composée de professionnels de santé à votre écoute du diagnostic, y compris des tumeurs du sein héréditaires, rares ou complexes, jusqu’aux traitements les plus innovants.
L’ICL propose un suivi permanent, depuis la prise en charge jusqu’à la fin du traitement, grâce à la mise en place d’un plan personnalisé de soins (PPS). Puis, après le traitement grâce à un programme personnalisé de l’après-cancer (PPAC). Ce parcours a la particularité de pouvoir être coordonné et partagé avec le CHRU de Nancy et le CH de Lunéville, permettant de proposer aux femmes et aux hommes de toute la région une prise en charge adaptée à leur situation.
Les patients au cœur d’un dispositif adapté et personnalisé.
Qu'est-ce que le cancer du sein ?
En chiffres
Le cancer du sein est le cancer le plus fréquent chez la femme, avec plus de 58 000* nouveaux cas chaque année en France. Près de 80% des cancers du sein se développent après 50 ans*. L’ICL prend en charge près de 1 390 nouveaux cas de cancer du sein chaque année.
*données Inca
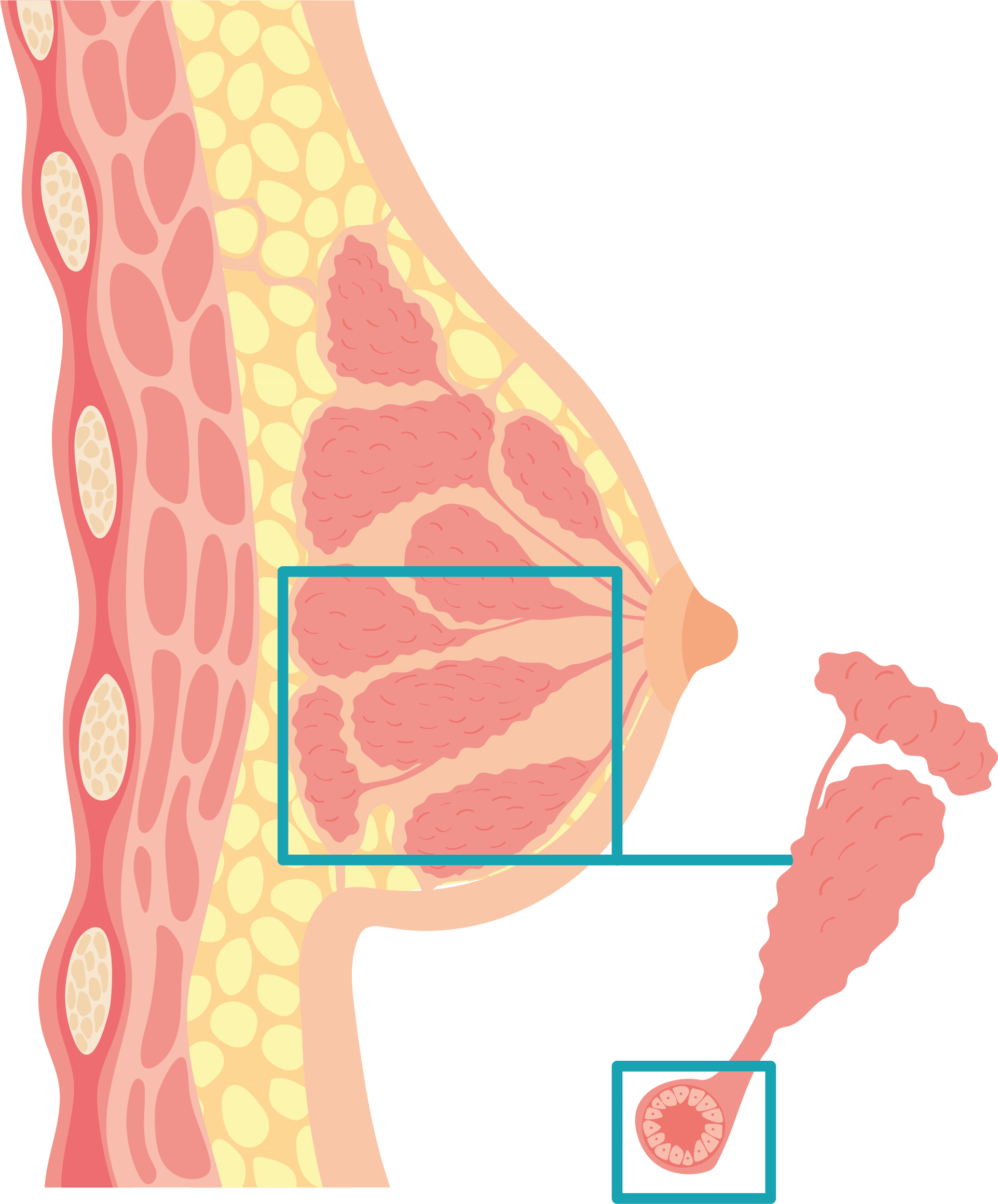
Canaux des glandes mammaire

Cellules normales d'un canal

Cellules avec cancer canalaire in situ

Cellules avec cancer canalaire infiltrant
Les facteurs de risque principaux du cancer du sein
Le cancer du sein est une maladie multifactorielle, cela signifie que plusieurs facteurs influent sur le risque de sa survenue. Un facteur de risque est tout élément qui, seul ou combiné à d’autres, augmente la probabilité d’engendrer des effets négatifs sur la santé de la population exposée. Les facteurs de risque peuvent être individuels, technologiques, sociaux, économiques, environnementaux ou politiques.
Pour le cancer du sein, les principaux facteurs de risque identifiés sont :
- L’âge, près de 80% des cancers se développent à partir de 50 ans.
- Des facteurs liés au mode de vie : le surpoids surtout après la ménopause, la sédentarité, l’absence d’activité physique, certaines habitudes de vie (alimentation, alcool, de tabac, etc.)
- Inactivité physique et sédentarité
- Antécédents personnels ou familiaux
- Des facteurs hormonaux : âge des premières règles et de la ménopause, âge à la première grossesse, nombre d’enfants.
Les signes ou symptômes d’alerte du cancer du sein
L’apparition ou la persistance d’un de ces symptômes doit conduire à consulter un médecin :
- Une boule ou masse dans un sein, en général non douloureuse et le plus souvent de consistance dure,
- Des ganglions durs et non douloureux à l’aisselle,
- Des modifications de la peau, de l’aspect, de la forme, de la taille du sein et du mamelon.
L’Institut de Cancérologie de Lorraine est classé 3ème en région Grand Est* et 18ème sur 326 hôpitaux en France* concernant la prise en charge des cancers du sein.
*palmarès Le Point des hôpitaux 2021
Dépistage du cancer du sein
Le dépistage organisé du cancer du sein s’adresse aux femmes de 50 à 74 ans tous les 2 ans. Le Centre régional de coordination des dépistages des cancers de votre région (CRCDC) adresse une invitation à participer à ce dépistage. Le dépistage est pris en charge à 100% et la 2e lecture systématique des mammographies normales est assurée par un second radiologue expérimenté. Le dépistage individuel du cancer du sein se fait sur avis médical.
Le dépistage des cancers du sein repose sur une mammographie, associée à un examen clinique des seins (observation et palpation).
Se faire dépister à l’ICL ? C’est possible en prenant rendez-vous directement 03 83 59 83 00
Auto-compression mammaire, autopalpation mammaire, CRCDC Grand Est, BRCA,…Ces termes vous évoquent vaguement quelque chose ? Pour en savoir plus, consultez notre lexique “les mots pour comprendre” sur la prévention du cancer du sein.
Ce diagnostic nécessite d’être explicité et un plan de traitement doit être établi. Pour ce faire, le dossier sera présenté en en réunion de concertation pluridisciplinaire (RCP).
Lors d’une consultation, l’annonce et les explications de la décision prise en RCP sont exposées au patient et à ses proches. Plusieurs possibilités de traitements sont alors envisageables : traitements médicaux (chimiothérapie, hormonothérapie, thérapies ciblées, immunothérapie), radiothérapie et/ou chirurgie.
Chirurgie du cancer du sein
Si les techniques de radiologie interventionnelle ne peuvent parvenir à prélever une tumeur, une chirurgie à visée diagnostique peut être proposée. Elle consiste à effectuer des prélèvements pour identifier précisément la nature de la tumeur par une analyse anatomopathologique (au microscope) pour déterminer la présence ou non de cellules cancéreuses et le cas échéant le type de tumeur.
La chirurgie à visée curative a pour but de retirer la tumeur avec une marge périphérique de sécurité. Elle est souvent associée au prélèvement des ganglions lymphatiques qui drainent le sein (ganglions axillaires). La chirurgie à visée curative peut être radicale ou conservatrice :
- Lorsqu’elle est dite radicale, dans le cadre du cancer du sein on parle alors de l’ablation du sein ou de mastectomie totale. Lorsque cela est possible une reconstruction mammaire immédiate (dans le même temps opératoire) ou différée pourra être proposée.
- Lorsque cela est compatible avec le stade de la tumeur, les chirurgiens procèdent à une intervention dite conservatrice. On parle de mastectomie partielle ou tumorectomie.
Le but du traitement chirurgical est d’assurer un contrôle local de la maladie (en enlevant toute la tumeur avec des marges de sécurité suffisantes) avec le moins de séquelles possibles. La décision est discutée entre le patient et le chirurgien avant l’opération.
En cas de maladie localisée, une procédure de ganglion sentinelle est associée à la chirurgie mammaire. Elle consiste en la détection et le retrait des premiers relais ganglionnaires du sein (1 à 3 ganglion(s) en moyenne) situés dans l’aisselle. Les ganglions sont ensuite analysés (analyse anatomopathologique) pour identifier la présence ou non de cellules cancéreuses. La procédure de ganglion sentinelle permet de limiter le risque de lymphoedème ou « gros bras » et l’inconfort au niveau de l’aisselle.
Une nouvelle intervention chirurgicale peut s’avérer nécessaire lorsque l’atteinte des ganglions sentinelles est importante ou en cas d’échec de la procédure de ganglion sentinelle. On parle de curage ganglionnaire. La chaîne ganglionnaire responsable du drainage du sein est alors retirée au niveau de l’aisselle.
Cette intervention expose à un risque de lymphoedème. Il peut se manifester après la chirurgie ou à distance. En cas d’apparition d’un lymphoedème, il faut rapidement consulter pour bénéficier de mesures adaptées. Ces mesures permettent souvent une régression partielle ou totale du lymphoedème.
Après une chirurgie mammaire, une activité physique adaptée pourra être entreprise.
On appelle chirurgie prophylactique la chirurgie pratiquée à titre préventif.
La chirurgie prophylactique mammaire est envisagée pour certaines femmes présentant une mutation des gènes BRCA1 ou BRCA2 qui prédisposent aux cancers du sein et de l’ovaire. D’autres mutations peuvent être incriminées. Cette intervention est envisagée après avis du service d’oncogénétique. Un délai de réflexion est nécessaire et une consultation auprès d’un psychologue est proposée. Dans ces indications, la qualité de vie liée au résultat fonctionnel postopératoire doit être mise en balance avec l’estimation des risques du cancer que l’on veut prévenir et avec l’alternative d’une surveillance rapprochée.
La chirurgie mammaire peut entraîner des séquelles esthétiques qui impactent la qualité de vie.
La chirurgie reconstructrice ou réparatrice est un moyen d’y remédier. La reconstruction mammaire fait partie intégrante de la prise en charge du cancer du sein, en particulier après une chirurgie mammaire non conservatrice (ou mastectomie).
La reconstruction mammaire se fait parfois en même temps que la chirurgie du cancer, on parle dans ce cas de reconstruction immédiate. Lorsqu’elle est réalisée après la fin des traitements, au cours d’une nouvelle intervention, on parle cette fois de reconstruction différée, ou de reconstruction secondaire.
Au cours de la consultation et après un examen, le chirurgien fait part aux patients des techniques les mieux adaptées à la situation et leur fournit une documentation détaillée. Un temps de réflexion est toujours proposé afin de se familiariser avec les options proposées.
Chaque patiente peut opter ou non pour une reconstruction mammaire. En l’absence de reconstruction, certaines femmes choisissent de porter une prothèse externe.
Traitements médicaux
Une chimiothérapie n’est pas proposée de façon systématique à tous les patients atteints d’un cancer du sein. Il s’agit de médicaments le plus souvent par voie injectable. Dans ce cas, il sera nécessaire d’organiser la pose d’un accès veineux central (le plus souvent, ce qu’on appelle une chambre à cathéter implantable). Ces médicaments agissent en bloquant les cellules en division. La chimiothérapie agit dans l’ensemble de l’organisme aussi bien au niveau de la tumeur primitive que sur les cellules disséminées dans le corps. Son action n’est pas spécifique c’est-à-dire qu’elle agit sur l’ensemble des cellules tumorales où qu’elles soient dans l’organisme mais aussi sur les cellules saines qui se divisent, ce qui explique les effets secondaires.
Chimiothérapie/chirurgie
La chimiothérapie adjuvante est proposée après la chirurgie. Elle est indiquée notamment lorsque l’examen anatomopathologique révèle que le risque de récidive est significatif. Elle a alors pour objectif de réduire ce risque et d’améliorer les chances de guérison. La chimiothérapie néo-adjuvante est proposée avant la chirurgie. Elle a pour objectif de réduire la taille d’une tumeur trop volumineuse pour être opérée d’emblée ou pour permettre une chirurgie conservatrice. Elle est également prescrite en cas de tumeur inflammatoire ou avec un profil biologique agressif.
Critères décisifs à l’indication de la chimiothérapie
L’indication de chimiothérapie est retenue en fonction des caractéristiques anatomopathologiques (c’est-à-dire de la tumeur vue au microscope) permettant d’évaluer le risque de récidive ou d’évolution de la maladie, et des caractéristiques biologiques (expression ou non de récepteurs hormonaux, surexpression ou non de HER2).
Plus la maladie est agressive, plus les risques de récidive sont élevés, plus la chimiothérapie est indiquée. Une surexpression d’HER2 nécessite la prescription d’une thérapie ciblée qui est systématiquement associée à une chimiothérapie, qu’elle soit administrée avant ou après la chirurgie. L’absence d’expression de récepteurs hormonaux et de surexpression d’HER2 (tumeurs dites « triple négatives ») nécessite la prescription d’une chimiothérapie.
Avant de proposer une chimiothérapie, le médecin tient également compte de l’état général des patients, de leur âge et antécédents.
Un test génomique peut être proposé en cas de situation dite « intermédiaire ». Selon le résultat, la chimiothérapie peut être évitée. Ces tests dits prédictifs reposent sur la recherche de marqueurs biologiques pronostiques ou prédictifs sur un échantillon de la tumeur.
Mesure des bénéfices de la chimiothérapie
Les bénéfices de la chimiothérapie ne sont pas « mesurables » individuellement. Ils sont reconnus à partir d’études sur une large population. Dans certaines situations, la prise de décision peut être complexe. Cela nécessite alors d’évaluer les risques : certains patients peuvent, de par leur âge, leurs antécédents, leurs maladies associées, présenter un risque de toxicité plus élevé.
Évaluation de l’efficacité de la chimiothérapie
Il n’y a pas, à ce jour, d’examens complémentaires permettant d’affirmer ou non l’efficacité de la chimiothérapie adjuvante (l’exérèse de la tumeur a été réalisée et le bilan d’extension n’a pas décelé de métastases : il n’y a donc aucune cible évaluable).
En cas de chimiothérapie néo-adjuvante, la taille de la tumeur +/- des ganglions axillaires est évaluée à chaque venue. Elle est confirmée en cours de traitement par une évaluation radiologique (mammographie, échographie), et elle est évaluée par l’analyse anatomopathologique après l’exérèse chirurgicale de la tumeur. Celle-ci peut conclure à une réponse complète signifiant l’absence de cellules tumorales résiduelles.
Il s’agit d’anticorps monoclonaux conçus spécialement pour bloquer la protéine HER2 qui a la propriété de favoriser la croissance des cellules. Certains cancers du sein ont la particularité de présenter à la surface de leurs cellules cancéreuses une quantité très importante de protéine HER2. On dit qu’elles sur-expriment HER2.
En agissant sur le récepteur HER2, cette thérapie permet de bloquer un des processus de division et de développement des cellules tumorales.
Son administration peut se faire par voie intra-veineuse ou par voie sous-cutanée.
L’hormonothérapie est utilisée pour traiter les cancers du sein hormonosensibles, en particulier aux oestrogènes.
L’hormonothérapie ne peut être prescrite que dans le cas de présence des récepteurs hormonaux lors de l’analyse anatomopathologique. Le type de traitement dépend du fait que la patiente soit ménopausée ou non.
Il existe deux types d’hormonothérapie. Ces traitements empêchent les cellules cancéreuses qui possèdent des récepteurs aux oestrogènes d’être stimulées par les oestrogènes de l’organisme :
- soit en entravant leur fixation, on parle alors d’anti-oestrogènes ;
- soit en empêchant leur production par inhibition enzymatique, on parle alors d’anti-aromatase.
Le terme hormonothérapie peut prêter à confusion et laisser penser à une thérapie à base d’hormones alors qu’au contraire il s’agit d’un traitement antihormonal. Les traitements à base d’hormones tels que les contraceptifs ou encore le traitement hormonal substitutif de la ménopause sont quant à eux contre-indiqués chez les patientes ayant été traitées pour un cancer du sein.
Ainsi l’hormonothérapie aura pour but de limiter l’interaction entre les hormones (oestrogènes et progestérone) circulant dans l’organisme et les récepteurs hormonaux qui sont des protéines situées sur le noyau des cellules cancéreuses dans les cancers du sein hormonosensibles. Cela va, par conséquent, éviter de stimuler le développement de ces cellules cancéreuses et les faire disparaître. C’est donc un traitement préventif des rechutes locales ou à distance (diminution du risque de récidive de 50 à 70% selon les études) jouant un rôle important dans le pronostic des patientes éligibles à cette thérapeutique.
80% des cancers du sein sont porteurs de récepteurs hormonaux et sont dits hormonosensibles ou hormonodépendants. Les cancers du sein ne possédant pas de récepteurs hormonaux (seuil fixé à 10% en France) ne sont pas candidats à l’hormonothérapie, car ils ne sont pas influencés par les hormones. Pour la majorité des patientes, l’hormonothérapie est prescrite en situation adjuvante c’est à dire après la fin des traitements locorégionaux que sont la chirurgie et la radiothérapie. Dans certains cas inopérables d’emblée, l’hormonothérapie peut être débutée au diagnostic.
Chez les patientes nécessitant une chimiothérapie + une thérapie ciblée (exemple : trastuzumab), l’hormonothérapie peut être débutée en même temps que la thérapie ciblée. L’hormonothérapie est poursuivie sur une durée minimale de 5 ans. Dans certains contextes, en fonction des caractéristiques tumorales et de la tolérance du traitement, l’oncologue peut prolonger la durée de l’hormonothérapie au-delà de 5 ans.
La régularité de la prise du médicament pendant toute la durée recommandée est très importante pour obtenir une bonne efficacité.
Une modification du traitement peut être effectuée en cours de route chez les patientes changeant de statut ménopausique ou en cas d’intolérance. Il existe différentes classes d’hormonothérapies utilisables en fonction du statut ménopausique avec un mécanisme d’action différent mais une finalité identique : le tamoxifène, les inhibiteurs de l’aromatase, les analogues de la LHRH.
L’immunothérapie ne consiste pas à détruire directement la tumeur, mais repose sur l’utilisation du système immunitaire, le mécanisme de défense de notre organisme contre les agents pathogènes comme les virus et les bactéries, ou les maladies telles que le cancer.
Le principe est de déverrouiller le système immunitaire pour qu’il puisse de nouveau combattre les cellules cancéreuses. En effet, les cellules tumorales sont capables de détourner à leur profit les dispositifs de contrôle du système immunitaire, ce qui leur permet de « désactiver » certaines cellules immunitaires et plus particulièrement, les lymphocytes T. L’organisme ne peut alors plus lutter contre la prolifération des cellules cancéreuses.
Des éléments clefs de ces mécanismes de blocage du système immunitaire, appelés « points de contrôle » (le récepteur PD-1 sur la cellule immunitaire et la protéine PDL1 sur la cellule cancéreuse,entre autres) peuvent être contrés par des traitements appelés « inhibiteurs de points de contrôle immunitaire ». Le déblocage de ces freins réactive alors le système immunitaire pour lui permettre de lutter contre les cellules cancéreuses.
Elle est proposée pour les tumeurs du sein dites « triple négatives » c’est-à-dire n’exprimant pas les récepteurs hormonaux, ni la protéine HER2. Elle est prescrite en association à une chimiothérapie, avant la chirurgie et peut être poursuivie après selon ce qu’on appelle la réponse histologique. Elle s’administre par voie intraveineuse toutes les 3 semaines. Les effets secondaires sont spécifiques et nécessitent une surveillance qui sera réalisée par l’oncologue à chaque venue.
Radiothérapie du cancer du sein
La radiothérapie consiste à utiliser des rayonnements (on dit aussi rayons ou radiations) pour détruire les cellules cancéreuses en bloquant leur capacité à se multiplier. On parle d’un traitement locorégional des cancers.
L’objectif de la radiothérapie consiste à irradier le foyer tumoral, à doses fractionnées, par des séances répétées, durant plusieurs jours à plusieurs semaines. Le traitement cible le plus précisément possible la zone à irradier pour protéger les organes sains situés à proximité de la tumeur.
Les techniques de radiothérapie utilisées aujourd’hui permettent de faire correspondre le plus précisément possible (de conformer) le volume sur lequel vont être dirigés les rayons, au volume de la tumeur.
La technique de radiothérapie externe la plus utilisée aujourd’hui est la radiothérapie conformationnelle 3D (trois dimensions).
Elle utilise des images en 3D de la tumeur et des organes avoisinants obtenues par scanner. Des logiciels permettent de simuler virtuellement, toujours en 3D, la forme des faisceaux d’irradiation et la distribution des doses. Cela permet de délivrer des doses efficaces de rayons en limitant l’exposition des tissus sains.
Cette technique consiste à faire varier la forme du faisceau au cours d’une même séance pour s’adapter précisément au volume à traiter, et ce même s’il comporte des « creux » ou des concavités (une tumeur en forme de fer à cheval située autour de la moelle épinière par exemple).
Il est possible d’avoir recours à une technique de radiothérapie asservie à la respiration qui permet d’éloigner le cœur de la zone traitée et de diminuer ainsi la dose délivrée au cœur, mais également aux poumons. Cette technique est utilisée dans les cas où la dose délivrée, notamment au niveau du cœur, nécessite d’être minimisée (selon l’étendue des zones traitées et/ou selon les pathologies et risques cardiaques présentés par le patient).
Il s’agit d’une technique de haute précision basée sur l’utilisation de microfaisceaux convergents permettant d’irradier à haute dose de très petits volumes.
Le Cyberknife®
C’est un système de radiochirurgie qui utilise la robotique pour traiter des tumeurs dans tout le corps. Elle consiste en un petit accélérateur linéaire, tenu par un robot capable de le déplacer dans toutes les directions possibles. Les faisceaux produits par cet appareil sont assez petits, mais ils peuvent être multipliés quasiment à l’infini et varier tous les angles de tir. Cela permet de focaliser la dose d’irradiation en minimisant l’impact sur les tissus sains avoisinants. Cette technique permet de traiter des tumeurs en place de taille limitée mais elle n’est en général pas utile pour les cancers du sein de présentation habituelle.
L’Institut de Cancérologie de Lorraine propose un parcours personnalisé et coordonné dans la prise en charge des cancers du sein.
Le parcours Sein permet de proposer aux personnes pour lesquelles une maladie du sein est suspectée d’avoir un diagnostic rapide. Les patients sont pris en charge par une équipe pluridisciplinaire spécialisée, composée de professionnels de santé à votre écoute du diagnostic, y compris des tumeurs du sein héréditaires, rares ou complexes, jusqu’aux traitements les plus innovants.
Un contact unique

Suspicion ou diagnostic de cancer du sein ?
Appelez le 03 83 59 83 00 pour une prise en charge dans des délais adaptés (de 8h à 18h du lundi au vendredi)